程序化细胞死亡(PCD, programmed cell death)在抗肿瘤治疗中具有广阔的应用前景。最新研究发现,肿瘤细胞的氧化失衡可导致细胞内的二硫化物应激(disulfide stress),从而引发细胞骨架蛋白的异常聚集,这种细胞死亡机制被称为“双硫死亡”(disulfidptosis)。诱导肿瘤细胞二硫化物应激和双硫死亡被认为是一种新兴的抗肿瘤策略。细胞质硒蛋白硫氧还蛋白还原酶(TXNRD1, thioredoxin reductase 1)是维持高等生物细胞内二硫化物稳态的关键酶,靶向TXNRD1以诱导双硫死亡的策略受到广泛关注。

近期,化工海洋与生命学院许建强课题组研究发现,天然二萜类化合物蓝萼甲素(Glaucocalyxin A,GlauA)在抗肿瘤治疗中具有显著的潜在价值。蓝萼甲素通过结合TXNRD1的Sec498残基,形成不可逆的共价加合物,从而抑制TXNRD1活性;蓝萼甲素显著耗竭了细胞内的谷胱甘肽(GSH),破坏了肿瘤细胞的氧化还原平衡,从而触发二硫化物应激,最终导致细胞死亡。这一发现为通过靶向TXNRD1诱导二硫化物应激作为新型抗肿瘤策略提供了实验证据。
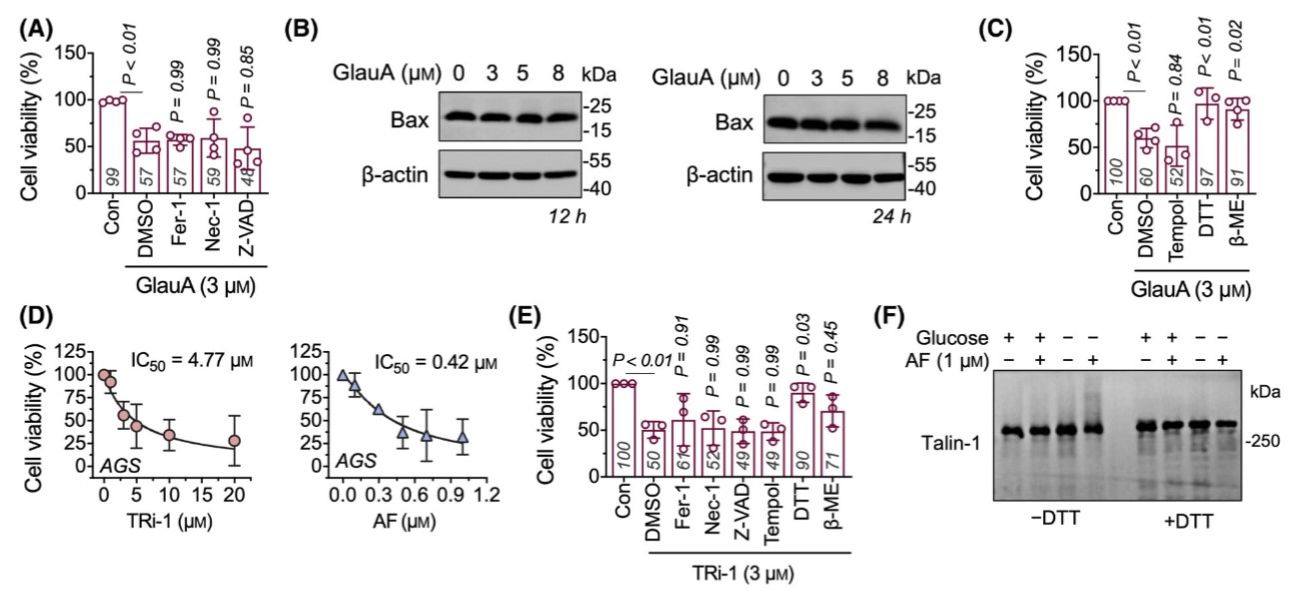
在肿瘤细胞中,TXNRD1作为关键的氧化还原酶负责维持细胞二硫化物的稳态,一旦TXNRD1功能受损,细胞内的二硫化物会异常累积,导致细胞骨架蛋白(如Talin-1)聚集,最终造成细胞结构崩溃和死亡。研究团队进一步发现,美国食品药品监督管理局(FDA)批准的TXNRD1抑制剂金诺芬(Auranofin)在胃癌细胞中促进了Talin-1蛋白的聚集,进一步支持了靶向TXNRD1诱导二硫化物应激的有效性。
该研究成果经同行评议、补充实验后,已经在国际学术期刊《FEBS Journal》发表。大连理工大学化工海洋与生命学院硕士生王令、课题组研究助理孙世博是文章的共同第一作者。硕士生柳昊雯、张秋雨、孟瑶参与此项研究工作,许建强副教授是文章的唯一通讯作者。
本研究项目受辽宁省科技厅联合基金(2023-MSBA-019)、辽宁省化学助剂合成与分离重点实验室项目(ZJFK2302)、大连理工大学中央高校基本科研业务费项目(DUT24MS019、DUT21LK29、DUT20LK36、DUT17JC36)、国家自然科学基金(U22A20455,31670767)等经费大力支持。
论文信息:
Ling Wang#, Shibo Sun#, Haowen Liu, Qiuyu Zhang, Yao Meng, Fan Sun, Jianjun Zhang, Haiyan Liu, Weiping Xu, Zhiwei Ye, Jie Zhang, Bingbing Sun, Jianqiang Xu*, Thioredoxin reductase inhibition and glutathione depletion mediated by glaucocalyxin A promote intracellular disulfide stress in gastric cancer cells, The FEBS Journal, 2024, 291(23):5276-5289. (中国科学院二区,JCR_Q1, SCI_IF_5.5) 文章链接 doi:10.1111/febs.17301
审核:王天舒